FRAKSI MINYAK BUMI
Minyak mentah (crude oil) sebagian besar tersusun dari senyawa-senyawa hidrokarbon jenuh (alkana). Adapun hidrokarbon tak jenuh (alkena, alkuna dan alkadiena) sangat sedikit dkandung oleh minyak bumi, sebab mudah mengalami adisi menjadi alkana.
Oleh karena minyak bumi berasal dari fosil organisme, maka minyak bumi mengandung senyawa-senyawa belerang (0,1 sampai 7%), nitrogen (0,01 sampai 0,9%), oksigen (0,6-0,4%) dan senyawa logam dalam jumlah yang sangat kecil. Minyak mentah dipisahkan menjadi sejumlah fraksi-fraksi melalui proses destilasi (penyulingan).
Pemisahan minyak mentah ke dalam komponen-komponen murni (senyawa tunggal) tidak mungkin dilakukan dan juga tidak prakstis sebab terlalu banyak senyawa yang ada dalam minyak tersebut dan senyawa hidrokarbon memiliki isomer-isomer dengan titik didih yang berdekatan.
Fraksi-fraksi yang diperoleh dari destilasi minyak bumi adalah campuran hidrokarbon yang mendidih pada trayek suhu tertentu. Misalnya fraksi minyak tanah (kerosin) tersusun dari campuran senyawa-senyawa yang mendidih antar 1800C-2500C. Proses destilasi dikerjakan dengan menggunakan kolom atau menara destilasi.
Proses pertama dalam pemrosesan minyak bumi adalah fraksionasi dari minyak mentah dengan menggunakan proses destilasi bertingkat, adapun hasil yang diperoleh adalah sebagai berikut:
- Minyak bisa menguap : minyak-minyak pelumas, lilin, parafin, dan vaselin.
- Bahan yang tidak bisa menguap : aspal dan arang minyak bumi
PENGOLAHAN MINYAK BUMI
Minyak bumi biasanya berada pada 3-4 km di bawah permukaan. Untuk mengambil minyak bumi tersebut harus dibuat sumur bor yang telah disesuaikan kedalamannya. Minyak mentah yang diperoleh ditampung dalam kapal tangker atau dialirkan ke kilang minyak dengan menggunakan pipa. Minyak mentah yang tadi diperoleh belum bisa dimanfaatkan sebagai bahan bakar maupun keperluan lainnya. Minyak mentah tersebut haruslah diolah terlebih dahulu.
Penyulingan Minyak Bumi
Minyak mentah mengandung sekitar 500 jenis hidrokarbon dengan jumlah atom C-1 hingga C-50. Pengolahan minyak bumi dilakukan melalui distilasi bertingkat, dimana minyak mentah dipisahkan ke dalam kelompok-kelompok dengan titik didih yang mirip. Hal tersebut dilakukan karena titik didih hidrokarbon meningkat seiring dengan bertambahnya atom karbon (C) dalam molekulnya. Mula mula minyak mentah dipanaskan pada suhu sekitar 400 0C. Setelah dipanaskan kemudian dialirkan ke tabung fraksionasi/ destilasi.
Menara destilasiDi menara inilah terjadi proses destilasi (penyulingan). Yaitu proses pemisahan larutan dengan menggunakan panas sebagai pemisah. Prinsip dasar penyulingan bertingkat adalah perbedaan titik didih di antara fraksi-fraksi minyak mentah. Jika selisih titik didih tidak berbeda jauh maka penyulingan tidak dapat diterapkan Hidrokarbon yang memiliki titik didih paling rendah akan terpisah lebih dulu, disusul dengan hidrokarbon yang memiliki titik didih lebih tinggi.
Destilasi Fraksinasi Minyak Bumi
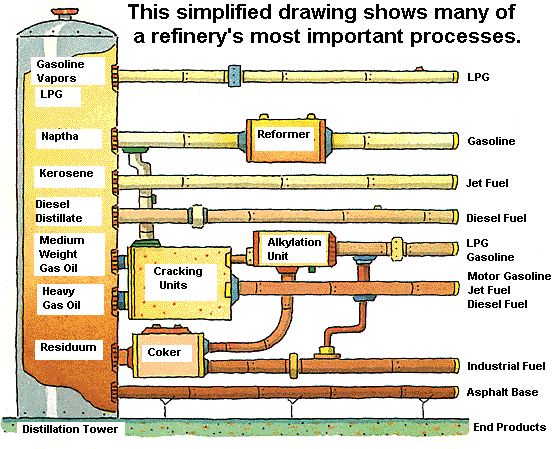
Meskipun komposisinya kompleks, terdapat cara mudah untuk memisahkan komponen-komponennya berdasarkan perbedaan nilai titik didihnya, yang disebut proses distilasi bertingkat. Destilasi merupakan pemisahan fraksi-fraksi minyak bumi berdasarkan perbedaan titik didihnya. Diagram pemisahan komponen-komponen minyak bumi dengan cara destilasi ditunjukkan oleh gambar di bawah ini :
Meskipun komposisinya kompleks, terdapat cara mudah untuk memisahkan komponen-komponennya berdasarkan perbedaan nilai titik didihnya, yang disebut proses distilasi bertingkat. Destilasi merupakan pemisahan fraksi-fraksi minyak bumi berdasarkan perbedaan titik didihnya. Diagram pemisahan komponen-komponen minyak bumi dengan cara destilasi ditunjukkan oleh gambar di bawah ini :
Minyak bumi atau minyak mentah sebelum masuk kedalam kolom fraksinasi (kolom pemisah) terlebih dahulu dipanaskan dalam aliran pipa dalam furnace (tanur) sampai dengan suhu ± 350°C. Minyak mentah yang sudah dipanaskan tersebut kemudian masuk kedalam kolom fraksinasi pada bagian flash chamber (biasanya berada pada sepertiga bagian bawah kolom fraksinasi).
Untuk menjaga suhu dan tekanan dalam kolom maka dibantu pemanasan dengan steam (uap air panas dan bertekanan tinggi).
Karena perbedaan titik didih setiap komponen hidrokarbon maka komponen-komponen tersebut akan terpisah dengan sendirinya, dimana hidrokarbon ringan akan berada dibagian atas kolom diikuti dengan fraksi yang lebih berat dibawahnya.
Pada tray (sekat dalam kolom) komponen itu akan terkumpul sesuai fraksinya masing-masing. Pada setiap tingkatan atau fraksi yang terkumpul kemudian dipompakan keluar kolom, didinginkan dalam bak pendingin, lalu ditampung dalam tanki produknya masing-masing. Produk ini belum bisa langsung dipakai, karena masih harus ditambahkan aditif (zat penambah).
Fraksi Minyak Bumi
Senyawa hidrokarbon, terutama parafinik dan aromatik, mempunyai trayek didih masing-masing, dimana panjang rantai hidrokarbon berbanding lurus dengan titik didih dan densitasnya. Semakin panjang rantai hidrokarbon maka trayek didih dan densitasnya semakin besar.
Jumlah atom karbon dalam rantai hidrokarbon bervariasi. Untuk dapat dipergunakan sebagai bahan bakar maka dikelompokkan menjadi beberapa fraksi atau tingkatan dengan urutan sederhana sebagai berikut:
- Gas
Rentang rantai karbon : C1 sampai C5
Trayek didih : 0 sampai 50°C - Gasolin (Bensin)
Rentang rantai karbon : C6 sampai C11
Trayek didih : 50 sampai 85°C - Kerosin (Minyak Tanah)
Rentang rantai karbon : C12 sampai C20
Trayek didih : 85 sampai 105°C - Solar
Rentang rantai karbon : C21 sampai C30
Trayek didih : 105 sampai 135°C - Minyak Berat
Rentang rantai karbon dari C31 sampai C40
Trayek didih dari 130 sampai 300°C - Residu
Rentang rantai karbon diatas C40
Trayek didih diatas 300°C
Kegunaan Fraksi-Fraksi Minyak Bumi
- Gas
Kegunaan: Gas tabung, BBG, umpan proses petrokomia. - Gasolin (Bensin)
Kegunaan : Bahan bakar motor, bahan bakar penerbangan bermesin piston, umpan proses petrokomia - Kerosin (Minyak Tanah)
Kegunaan: Bahan bakar motor, bahan bakar penerbangan bermesin jet, bahan bakar rumah tangga, bahan bakar industri, umpan proses petrokimia - Solar
Kegunaan: Bahan bakar motor, bahan bakar industry - Minyak Berat
Kegunaan: Minyak pelumas, lilin, umpan proses petrokimia - Residu
Kegunaan: Bahan bakar boiler (mesin pembangkit uap panas), aspal, bahan pelapis anti bocor.